Гибридизация электронных орбиталей и геометрия молекул. Гибридизация атомных орбиталей
Дипольные моменты молекул
Метод валентных связей основывается на положении, что каждая пара атомов в химической частице удерживается вместе при помощи одной или нескольких электронных пар. Эти пары электронов принадлежат двум связываемым атомам и локализованы в пространстве между ними. За счет притяжения ядер связываемых атомов к этим электронам и возникает химическая связь.
Перекрывание атомных орбиталей
При описании электронного строения химической частицы электроны, в том числе и обобществленные, относят к отдельным атомам и их состояния описывают атомными орбиталями. При решении уравнения Шредингера приближенную волновую функцию выбирают так, чтобы она давала минимальную электронную энергию системы, то есть наибольшее значение энергии связи. Это условие достигается при наибольшем перекрывании орбиталей, принадлежащей одной связи. Таким образом, пара электронов, связывающих два атома, находится в области перекрывания их атомных орбиталей.
Перекрываемые орбитали должны иметь одинаковую симметрию относительно межъядерной оси.
Перекрывание атомных орбиталей вдоль линии, связывающей ядра атомов, приводит к образованию σ-связей. Между двумя атомами в химической частице возможна только одна σ-связь. Все σ-связи обладают осевой симметрией относительно межъядерной оси. Фрагменты химических частиц могут вращаться вокруг межъядерной оси без нарушения степени перекрывания атомных орбиталей, образующих σ-связи. Совокупность направленных, строго ориентированных в пространстве σ-связей создает структуру химической частицы.
При дополнительном перекрывании атомных орбиталей, перпендикулярных линии связи, образуются π-связи.

В результате этого между атомами возникают кратные связи:
| Одинарная (σ) | Двойная (σ +π) | Тройная (σ + π + π) |
| F−F | O=O | N≡N |
С появлением π-связи, не имеющей осевой симметрии, свободное вращение фрагментов химической частицы вокруг σ-связи становится невозможным, так как оно должно привести к разрыву π-связи. Помимо σ- и π-связей, возможно образование еще одного вида связи - δ-связи:

Обычно такая связь образуется после образования атомами σ- и π-связей при наличии у атомов d
- и f
-орбиталей путем перекрывания их "лепестков" сразу в четырех местах. В результате кратность связи может возрасти до 4-5.
Например, в октахлородиренат(III)-ионе 2- между атомами рения образуются четыре связи.
Механизмы образования ковалентных связей
Различают несколько механизмов образования ковалентной связи: обменный (равноценный), донорно-акцепторный , дативный .
При использовании обменного механизма образование связи рассматривается как результат спаривания спинов свободных электронов атомов. При этом осуществляется перекрывание двух атомных орбиталей соседних атомов, каждая из которых занята одним электроном. Таким образом, каждый из связываемых атомов выделяет для обобществления пары по электрону, как бы обмениваясь ими. например, при образовании молекулы трифторида бора из атомов три атомные орбитали бора, на каждой из которых имеется по одному электрону, перекрываются с тремя атомными орбиталями трех атомов фтора (на каждой из них также находится по одному неспаренному электрону). В результате спаривания электронов в областях перекрывания соответствующих атомных орбиталей появляется три пары электронов, связывающих атомы в молекулу.
По донорно-акцепторному механизму перекрывается орбиталь с парой электронов одного атома и свободная орбиталь другого атома. В этом случае в области перекрывания также оказывается пара электронов. По донорно-акцепторному механизму происходит, например, присоединение фторид-иона к молекуле трифторида бора. Вакантная р -орбиталь бора (акцептора электронной пары) в молекуле BF 3 перекрывается с р -орбиталью иона F − , выступающего в роли донора электронной пары. В образовавшемся ионе − все четыре ковалентные связи бор−фтор равноценны по длине и энергии, несмотря на различие в механизме их образования.
Атомы, внешняя электронная оболочка которых состоит только из s - и р -орбиталей, могут быть либо донорами, либо акцепторами электронной пары. Атомы, у которых внешняя электронная оболочка включает d -орбитали, могут выступать в роли и донора, и акцептора пар электронов. В этом случае рассматривается дативный механизм образования связи. Примером проявления дативного механизма при образования связи служит взаимодействие двух атомов хлора. Два атома хлора в молекуле Cl 2 образуют ковалентную связь по обменному механизму, объединяя свои неспаренные 3р -электроны. Кроме того, происходит перекрывание 3р -орбитали атом Cl-1, на которой имеется пара электронов, и вакантной 3d -орбитали атома Cl-2, а также перекрывание 3р -орбитали атом Cl-2, на которой имеется пара электронов, и вакантной 3d -орбитали атома Cl-1. Действие дативного механизма приводит к увеличению прочности связи. Поэтому молекула Cl 2 является более прочной, чем молекула F 2 , в которой ковалентная связь образуются только по обменному механизму:
Гибридизация атомных орбиталей
При определении геометрической формы химической частицы следует учитывать, что пары внешних электронов центрального атома, в том числе и не образующие химическую связь, располагаются в пространстве как можно дальше друг от друга.
При рассмотрении ковалентных химических связей нередко используют понятие о гибридизации орбиталей центрального атома - выравнивание их энергии и формы. Гибридизация является формальным приемом, применяемым для квантово-химического описания перестройки орбиталей в химических частицах по сравнению со свободными атомами. Сущность гибридизации атомных орбиталей состоит в том, что электрон вблизи ядра связанного атома характеризуется не отдельной атомной орбиталью, а комбинацией атомных орбиталей с одинаковым главным квантовым числом. Такая комбинация называется гибридной (гибридизованной) орбиталью. Как правило, гибридизация затрагивает лишь высшие и близкие по энергии атомные орбитали, занятые электронами.
В результате гибридизации появляются новые гибридные орбитали (рис.24), которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары (или неспаренные электроны) оказались максимально удаленными друг от друга, что соответствует минимуму энергии межэлектронного отталкивания. Поэтому тип гибридизации определяет геометрию молекулы или иона.
ТИПЫ ГИБРИДИЗАЦИИ
| Тип гибридизации | Геометрическая форма | Угол между связями | Примеры |
| sp | линейная | 180 o | BeCl 2 |
| sp 2 | треугольная | 120 o | BCl 3 |
| sp 3 | тетраэдрическая | 109,5 o | CH 4 |
| sp 3 d | тригонально-бипирамидальная | 90 o ; 120 o | PCl 5 |
| sp 3 d 2 | октаэдрическая | 90 o | SF 6 |

В гибридизации участвуют не только связывающие электроны, но и неподеленные электронные пары. Например, молекула воды содержит две ковалентные химические связи между атомом кислорода и двумя атомами водорода.
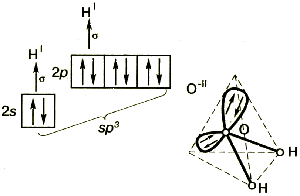
Помимо двух пар электронов, общих с атомами водорода, у атома кислорода имеются две пары внешних электронов, не участвующих в образовании связи (неподеленные электронные пары). Все четыре пары электронов занимают определенные области в пространстве вокруг атома кислорода.
Поскольку электроны отталкиваются друг от друга, электронные облака располагаются на возможно большем расстоянии друг от друга. При этом в результате гибридизации меняется форма атомных орбиталей, они вытянуты и направлены к вершинам тетраэдра. Поэтому молекула воды имеет угловую форму, а угол между связями кислород-водород равен 104,5 o .
Для предсказания типа гибридизации удобно использовать донорно-акцепторный механизм образования связи: происходит перекрывание пустых орбиталей менее электроотрицательного элемента и орбиталей более электроотрицательного элемента с находящимися на них парами электронов. При составлении электронных конфигураций атомов учитывают их степени окисления − условное число, характеризующее заряд атома в соединении, рассчитанный исходя из предположения ионного строения вещества.
Чтобы определить тип гибридизации и форму химической частицы, поступают следующим образом:
Наличие π-связей не влияет на тип гибридизации. Однако наличие дополнительного связывания может привести к изменению валентных углов, поскольку электроны кратных связей сильнее отталкиваются друг от друга. По этой причине, например, валентный угол в молекуле NO 2 (sp 2 -гибридизация) увеличивается от 120 o до 134 o .

Кратность связи азот−кислород в этой молекуле равна 1,5, где единица отвечает одной σ-связи, а 0,5 равно отношению числа орбиталей атома азота, не участвующих в гибридизации (1) к числу оставшихся активных электронных пар у атома кислорода, образующих π-связи (2). Таким образом, наблюдается делокализация π-связей (делокализованные связи − ковалентные связи, кратность которых не может быть выражена целым числом).
В случае sp , sp 2 , sp 3 , sp 3 d 2 гибридизации вершины в многограннике, описывающем геометрию химической частицы, равноценны, и поэтому кратные связи и неподеленные пары электронов могут занимать любые из них. Однако sp 3 d -гибридизации отвечает тригональная бипирамида , в которой валентные углы для атомов, расположенных в основании пирамиды (экваториальной плоскости), равны 120 o , а валентные углы с участием атомов, расположенных в вершинах бипирамиды, равны 90 o . Эксперимент показывает, что неподеленные электронные пары всегда располагаются в экваториальной плоскости тригональной бипирамиды. На этом основании делается вывод, что они требуют больше свободного пространства, чем пары электронов, участвующие в образовании связи. Примером частицы с таким расположением неподеленной электронной пары является тетрафторид серы (рис. 27). Если центральный атом одновременно имеет неподеленные пары электронов и образует кратные связи (например, в молекуле XeOF 2), то в случае sp 3 d -гибридизации именно они располагаются в экваториальной плоскости тригональной бипирамиды (рис. 28).
Дипольные моменты молекул
Идеальная ковалентная связь существует лишь в частицах, состоящих из одинаковых атомов (Н 2 , N 2 и т.д.). Если образуется связь между различными атомами, то электронная плотность смещается к одному из ядер атомов, то есть происходит поляризация связи. Характеристикой полярности связи служит ее дипольный момент.
Дипольный момент молекулы равен векторной сумме дипольных моментов ее химических связей (с учетом наличия неподеленных пар электронов). Если полярные связи расположены в молекуле симметрично, то положительные и отрицательные заряды компенсируют друг друга, и молекула в целом является неполярной. Так происходит, например, с молекулой диоксида углерода. Многоатомные молекулы с несимметричным расположением полярных связей (и, следовательно, электронной плотности) являются в целом полярными. Это относится, в частности, к молекуле воды.
На результирующее значение дипольного момента молекулы может повлиять неподеленная пара электронов. Так, молекулы NH 3 и NF 3 имеют тетраэдрическую геометрию (с учетом неподеленной пары электронов). Степени ионности связей азот−водород и азот−фтор составляют 15 и 19%, соответственно, а их длины - 101 и 137 пм, соответственно. Исходя из этого, можно было бы сделать вывод о большем дипольном моменте NF 3 . Однако эксперимент показывает обратное. При более точном предсказании дипольного момента следует учитывать направление дипольного момента неподеленной пары (рис. 29).
Гибридизация атомных орбиталей и геометрия молекул
Важной характеристикой молекулы, состоящей более чем из двух атомов, является ее геометрическая конфигурация. Она определяется взаимным расположением атомных орбиталей, участвующих в образовании химических связей.
Перекрывание электронных облаков возможно только при определенной взаимной ориентации электронных облаков; при этом область перекрывания располагается в определенном направлении по отношению к взаимодействующим атомам.
Таблица 1 Гибридизация орбиталей и пространственная конфигурация молекул
Возбужденный атом бериллия имеет конфигурацию 2s 1 2p 1 , возбужденный атом бора - 2s 1 2p 2 и возбужденный атом углерода - 2s 1 2p 3 . Поэтому можно считать, что в образовании химических связей могут участвовать не одинаковые, а различные атомные орбитали. Например, в таких соединениях как BeCl 2 , BeCl 3 ,CCl 4 должны быть неравноценные по прочности и направлению связи, причем σ-связи из p-орбиталей должны быть более прочными, чем связи из s-орбиталей, т.к. для p-орбиталей имеются более благоприятные условия для перекрывания. Однако опыт показывает, что в молекулах, содержащих центральные атомы с различными валентными орбиталями (s, p, d), все связи равноценны. Объяснение этому дали Слейтер и Полинг. Они пришли к выводу, что различные орбитали, не сильно отличающиеся по энергиям, образуют соответствующее число гибридных орбиталей. Гибридные (смешанные) орбитали образуются из различных атомных орбиталей. Число гибридных орбиталей равно числу атомных орбиталей, участвующих в гибридизации. Гибридные орбитали одинаковы по форме электронного облака и по энергии. По сравнению с атомными орбиталями они более вытянуты в направлении образования химических связей и поэтому обусловливают лучшее перекрывание электронных облаков.
Гибридизация атомных орбиталей требует затрат энергии, поэтому гибридные орбитали в изолированном атоме неустойчивы и стремятся превратиться в чистые АО. При образовании химических связей гибридные орбитали стабилизируются. Вследствие более прочных связей, образованных гибридными орбиталями, из системы выделяется больше энергии, и поэтому система становится более стабильной.
sp–гибридизация имеет место, например, при образовании галогенидов Be, Zn, Co и Hg (II). В валентном состоянии все галогениды металлов содержат на соответствующем энергетическом уровне s и p-неспаренные электроны. При образовании молекулы одна s- и одна р-орбиталь образуют две гибридные sp-орбитали под углом 180 о.
Рис.3 sp-гибридные орбитали
Экспериментальные данные показывают, что все галогениды Be, Zn, Cd и Hg (II) линейны и обе связи имеют одинаковую длину.
sp 2 -гибридизация
В результате гибридизации одной s-орбитали и двух p-орбиталей образуются три гибридные sp 2 -орбитали, расположенные в одной плоскости под углом 120 о друг к другу. Такова, например, конфигурация молекулы BF 3:


Рис.4 sp 2 -гибридизация
sp 3 -гибридизация
sp 3 -гибридизация характерна для соединений углерода. В результате гибридизации одной s-орбитали и трех
р-орбиталей образуются четыре гибридные sp 3 -орбитали, направленные к вершинам тетраэдра с углом между орбиталями 109,5 о. Гибридизация проявляется в полной равноценности связей атома углерода с другими атомами в соединениях, например, в CH 4 , CCl 4 , C(CH 3) 4 и др.


Рис.5 sp 3 -гибридизация
Если все гибридные орбитали связаны с одинаковыми атомами, то связи ничем не отличаются друг от друга. В других случаях встречаются небольшие отклонения от стандартных валентных углов. Например, в молекуле воды H 2 O кислород - sp 3 -гибридный, находится в центре неправильного тетраэдра, в вершины которого "смотрят" два атома водорода и две неподеленные пары электронов (рис. 2). Форма молекулы угловая, если смотреть по центрам атомов. Валентный угол HОН составляет 105 о, что довольно близко к теоретическому значению 109 о.

Рис.6 sp 3 -гибридизация атомов кислорода и азота в молекулах а) H 2 O и б) NCl 3 .
Если бы не происходило гибридизации (“выравнивания” связей O-H), валентный угол HOH был бы равен 90°, потому что атомы водорода были бы присоединены к двум взаимно перпендикулярным р-орбиталям. В этом случае наш мир выглядел бы, вероятно, совершенно по-другому.
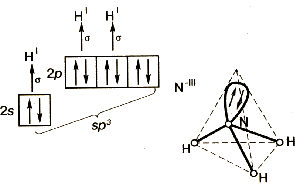
Теория гибридизации объясняет геометрию молекулы аммиака. В результате гибридизации 2s и трёх 2p орбиталей азота образуются четыре гибридные орбитали sp 3 . Конфигурация молекулы представляет из себя искажённый тетраэдр, в котором три гибридных орбитали участвуют в образовании химической связи, а четвёртая с парой электронов – нет. Углы между связями N-H не равны 90 о как в пирамиде, но и не равны 109,5 о, соответствующие тетраэдру.

Рис.7 sp 3 - гибридизация в молекуле аммиака
При взаимодействии аммиака с ионом водорода в результате донорно-акцепторного взаимодействия образуется ион аммония, конфигурация которого представляет собой тетраэдр.
Гибридизация объясняет также отличие угла между связями О-Н в угловой молекуле воды. В результате гибридизации 2s и трёх 2p орбиталей кислорода образуются четыре гибридных орбитали sp 3 , из которых только две участвуют в образовании химической связи, что приводит к искажению угла, соответсвующего тетраэдру.

Рис.8 sp 3 -гибридизация в молекуле воды
В гибридизацию могут включаться не только s- и р-, но и d- и f-орбитали.
При sp 3 d 2 -гибридизации образуется 6 равноценных облаков. Она наблюдается в таких соединениях как 4- , 4- . При этом молекула имеет конфигурацию октаэдра:

Рис. 9 d 2 sp 3 -гибридизация в ионе 4-
Представления о гибридизации дают возможность понять такие особенности строения молекул, которые не могут быть объяснены другим способом.
Гибридизация атомных орбиталей (АО) приводит к смещению электронного облака в направлении образования связи с другими атомами. В результате области перекрывания гибридных орбиталей оказываются больше, чем для чистых орбиталей и прочность связи увеличивается.
Одна из задач химии - это изучение строения вещества, в том числе выяснение механизма образования различных соединений из простых веществ, образуемых атомами одного химического элемента. Особенности взаимодействия атомов, точнее, их разноименно заряженных компонентов - электронных оболочек и ядер, - описываются как различные типы химической связи. Так, вещества, образуются посредством ковалентной связи, для описания которой в 1931 году американским химиком Л. Полингом была предложена модель гибридизации атомных орбиталей.
Понятие о ковалентной связи
В тех случаях, когда в процессе взаимодействия происходит образование общей для двух атомов пары валентных электронных облаков, говорят о ковалентной связи. В результате ее возникновения формируется мельчайшая частица простого или сложного вещества - молекула.
Одной из особенностей ковалентной связи является ее направленность - следствие сложной формы электронных орбиталей p, d и f, которые, не обладая сферической симметрией, имеют определенную пространственную ориентацию. Еще одна важная особенность данного типа химической связи - насыщаемость, обусловленная ограниченным количеством внешних - валентных - облаков в атоме. Именно поэтому существование молекулы, например, H 2 O, возможно, а H 5 O - нет.
Типы ковалентной связи
Образование общих электронных пар может происходить различными способами. В механизме образования ковалентной связи важную роль играет характер перекрытия облаков и пространственная симметрия результирующего облака. По данному критерию Л. Полинг предложил различать следующие типы:
- Сигма-связь (σ) отличается наибольшей степенью перекрытия по оси, проходящей через атомные ядра. Здесь плотность облака будет максимальной.
- Пи-связь (π) образуется при боковом перекрывании, и электронное облако, соответственно, имеет наибольшую плотность вне соединяющей ядра оси.

Эти пространственные характеристики имеют большое значение постольку, поскольку они коррелируют с энергетическими параметрами ковалентной связи.
Особенности многоатомных молекул
Концепция гибридизации была введена Полингом для объяснения одной из особенностей ковалентных связей в многоатомных молекулах. Известно, что связи, образуемые центральным атомом в таких молекулах, оказываются одинаковыми по пространственным и энергетическим характеристикам. Это происходит вне зависимости от того, какие орбитали (s, p или d) участвуют в формировании общей электронной пары.
Очень удобным и наглядным примером для иллюстрации этого явления служит атом углерода. При вступлении в химическую связь атом в возбужденном состоянии имеет 4 валентных орбитали: 2s, 2p x , 2p y и 2p z . Три последних отличаются от орбитали 2s по энергии и форме. Тем не менее в молекуле, например, метана CH 4 все четыре связи совершенно равноценны и имеют валентные углы 109,5° (в то время как p-орбитали расположены под углами 90°). В других соединениях углерода встречаются валентные углы 120° и 180°; в молекулах, содержащих азот (аммиак NH 3) и кислород (вода H 2 O) эти углы составляют 107,5° и 104,5°. Возникновение подобных валентных углов также потребовало объяснения.

Суть явления
Идея гибридизации состоит в образовании усредненных орбиталей путем перекрывания электронных облаков разного типа с близкими значениями энергии - s, p, иногда d. Количество результирующих - гибридных - орбиталей соответствует числу перекрывающихся облаков. Поскольку орбиталь - это определяющая вероятность нахождения электрона в той или иной точке атома, гибридная орбиталь представляет собой наложение волновых функций, происходящее в результате электронных переходов при возбуждении атома. Оно приводит к возникновению равнозначных волновых функций, различающихся только направленностью.
Гибридные орбитали эквивалентны по энергии и имеют одинаковую форму в виде объемной восьмерки, имеющей сильную асимметрию относительно ядра. На гибридизацию затрачивается меньше энергии, чем выделяется при образовании прочной ковалентной связи с гибридными орбиталями, поэтому такой процесс энергетически выгоден, то есть наиболее вероятен.

гибридизации орбиталей и геометрия молекул
Возможны различные варианты перекрывания (смешения) внешних электронных облаков в атоме. Самыми распространенными являются следующие виды наложения орбиталей:
- Sp 3 -гибридизация. Данный вариант реализуется при наложении одной s- и трех p-орбиталей. Результатом его становятся четыре гибридные орбитали, оси которых направлены для любой пары под углами 109,5°, соответствующим минимальному взаимному отталкиванию электронов. При вступлении этих орбиталей в σ-связи с другими атомами, формируется молекула тетраэдрической конфигурации, например, метан, этан C 2 H 6 (комбинация двух тетраэдров), аммиак, вода. В молекуле аммиака одна, а в молекуле воды - две из вершин тетраэдра заняты неподеленными электронными парами, что приводит к уменьшению валентного угла.
- Sp 2 -гибридизация возникает при комбинации одной s- и двух p-орбиталей. В этом случае тройка гибридных орбиталей располагается под углами 120° в одной плоскости. Подобную треугольную форму имеют, например, молекулы трихлорида бора BCl 3 , находящего применение в различных технологиях. Другой пример - молекула этилена - формируется за счет дополнительной π-связи между атомами углерода, в которых по одной p-орбитали негибридные и ориентированы перпендикулярно плоскости, образуемой двумя треугольниками.
- Sp-гибридизация происходит, когда смешиваются одна s- и одна p-орбиталь. Два гибридных облака располагаются под углом 180°, а молекула имеет линейную конфигурацию. Примерами могут служить молекулы хлорида бериллия BeCl 2 или ацетилена C 2 H 2 (в последней две негибридные p-орбитали углерода образуют дополнительные π-связи).

Существуют и более сложные варианты гибридизации атомных орбиталей: sp 3 d, sp 3 d 2 и другие.
Роль модели гибридизации
Концепция Полинга дает хорошее качественное описание строения молекул. Она удобна и наглядна, успешно объясняет некоторые особенности ковалентных соединений, такие как величина валентных углов или выравнивание длины химической связи. Однако количественная сторона модели не может считаться удовлетворительной, поскольку не позволяет делать многие важные предсказания, касающиеся физических эффектов, связанных с особенностями строения молекул, - например, молекулярных фотоэлектронных спектров. Сам автор концепции гибридизации уже в начале 1950-х годов отмечал ее недостатки.
Тем не менее в становлении современных представлений о строении вещества модель гибридизации атомных орбиталей сыграла большую роль. На основе ее были разработаны более адекватные концепции, например, теория отталкивания электронных пар. Поэтому, безусловно, модель гибридизации явилась важным этапом в развитии теоретической химии, а при описании некоторых аспектов электронной структуры молекул она вполне применима и в настоящее время.
| Одинарная (σ) | Двойная (σ+π) | Тройная (σ + π + π) |
| С–С С–Н С–О H–Cl | С=O С=С О=О | С≡С С≡N N≡N |
Гибридизация
Если атом связан с другими атомами ОДИНАКОВЫМИ СВЯЗЯМИ, но при их образовании участвуют орбитали разного типа, то используется метод ГИБРИДИЗАЦИИ.
Пример: Молекула СН 4 имеет форму правильного тетраэдра, в ней все 4 связи имеют одинаковую длину, прочность, находятся под одинаковыми углами друг к другу.
Однако у четырёхвалентного атома углерода электроны расположены на трёх р-орбиталях и одной s-орбитали. Они разные по энергии, форме и расположены в пространстве иначе.
Для объяснения используется понятие ГИБРИДИЗАЦИИ:
Из четырёх атомных орбиталей образуются 4 новых,
гибридных орбитали, которые в пространстве располагаются НА МАКСИМАЛЬНОМ УДАЛЕНИИ ДРУГ ОТ ДРУГА. Это правильный тетраэдр, углы между связями равны 109° 29´.
Так как в образовании четырёх связей участвуют одна s и три р-оболочки, то такой тип гибридизации обозначается sp 3
В зависимости от числа и типа орбиталей, которые принимают участие в гибридизации, отличают следующие типы гибридизации:
1) sp-гибридизация. Участвуют одна s-орбиталь и одна р-орбиталь. Молекула имеет линейную структуру, валентный угол – 180 0 .
2) sp 2 -гибридизация. Участвуют одна s-орбиталь и две р-орбитали. Молекула располагается в плоскости (концы гибридных орбиталей направлены к вершинам равностороннего треугольника), валентный угол – 120 0 .
3) sp 3 -гибридизация. Участвуют одна s-орбиталь и три р-орбитали. Молекула имеет тетраэдрическую форму, валентный угол – 109,28 0 .
Как определить тип гибридизации?
1. В гибридизации участвуют сигма-связи и НЕПОДЕЛЁННЫЕ ИОННЫЕ ПАРЫ.
2. Общее число участвующих орбиталей сигма-связей + электронных пар = числу гибридных орбиталей и определяет тип гибридизации.
Задание: определить тип гибридизации атома углерода в молекуле фосгена.
O=C – Cl
1) углерод образует 2 одинарные связи (это сигма-связи) и одну двойную связь (сигма+пи).Все 4 электрона углерода участвуют в образовании этих связей.
2) таким образом, в гибридизации примут участие ТРИ СИГМА-связи. Это sp 2 - гибридизация , молекула имеет форму плоского треугольника. Пи-связь располагается перпендикулярно плоскости этого треугольника.
Для объяснения фактов, когда атом образует большее число связей, чем число неспаренных электронов в его основном состоянии (например, атом углерода), используется постулат о гибридизации близких по энергии атомных орбиталей. Гибридизация АО происходит при образовании ковалентной связи , если при этом достигается более эффективное перекрывание орбиталей. Гибридизация атома углерода сопровождается его возбуждением и переносом электрона с 2s - на 2р -АО:
Основное и возбужденное состояния атома углерода.
Гибридизация АО - это взаимодействие (смешение) разных по типу, но близких по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии.
Например, смешение 2s-АО с 2p -АО дает две гибридные 2sp -АО:
АО с большой разницей в энергии (например, 1s и 2р ) в гибридизацию не вступают. В зависимости от числа участвующих в гибридизации p -АО возможны следующие виды гибридизации:
для атомов углерода и азота - sp 3 , sp 2 и sp ;
для атома кислорода - sp 3 , sp 2 ;
для галогенов - sp 3 .
Гибридная АО асимметрична и сильно вытянута в одну сторону от ядра (форма неправильной восьмерки).

В отличие от негибридных s - или р -АО, она имеет одну большую долю, которая хорошо образует химическую связь, и малую долю, которую обычно даже не изображают. Гибридизованные АО при взаимодействии с орбиталями различных типов (s -, р - или гибридными АО) других атомов обычно дают s-МО, т.е. образуют s-связи. Такая связь прочнее связи, образованной электронами негибридных АО, за счет более эффективного перекрывания.
3.3.1. sp 3 -Гибридизация (тетраэдрическая).
Одна s - и три р четыре равноценные по форме и энергии sp 3 -гибридные орбитали.
Орбитальная модель атома в sp 3 -гибридизованном состоянии.

Для атома углерода и других элементов 2-го периода этот процесс происходит по схеме:
2s + 2p x + 2p y + 2p z = 4 (2sp 3)

Схема sp 3 -гибридизации атомных орбиталей.
Оси sp 3 -гибридных орбиталей направлены к вершинам правильного тетраэдра. Тетраэдрический угол между ними равен 109°28", что соответствует наименьшей энергии отталкивания электронов.
Впервые идею о направленности единиц сродства (валентностей) атома углерода по углам тетраэдра независимо друг от друга выдвинули в 1874 г. Вант-Гофф и Ле Бель.
sp 3 -Орбитали могут образовывать четыре s-связи с другими атомами или заполняться неподеленными парами электронов.
А как наглядно изобразить пространственное строение атома в sp 3 -состоянии на рисунке?
В этом случае sp 3 -гибридные орбитали изображают не электронными облаками, а прямыми линиями или клиньями в зависимости от пространственной ориентации орбитали. Такое схематическое изображение используется при написании стереохимических (пространственных) формул молекул.

Переход от орбитальной модели (а) к пространственной формуле (б).
На примере молекулы метана показаны объемные модели и пространственная (стереохимическая) формула молекулы с sp 3 -углеродным атомом.



Модель молекулы метана
sp 3 -Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 4.
Углерод в sp 3 -гибридном состоянии встречается в простом веществе - алмазе. Это состояние характерно для атомов С, N, O и др., соединенных с другими атомами одинарными связями (sp 3 -атомы выделены красным цветом):
С H 4 , RC H 3 , N H 3 , RN H 2 , H 2 O , RO H, R 2 O ;
а также анионам типа:
R 3 C : - , RO - .
Следствием тетраэдрического строения sp 3 -атома является возможность существования двух оптических стереоизомеров у соединения, содержащего такой атом с четырьмя разными заместителями (Вант-Гофф, Ле Бель, 1874).
3.3.2. sp 2 -Гибридизация (плоскостно-тригональная).
Одна s - и две p -орбитали смешиваются, и образуются три равноценные sp 2 -гибридные орбитали, расположенные в одной плоскости под углом 120° (выделены синим цветом). Они могут образовывать три s-связи. Третья р -орбиталь остается негибридизованной и ориентируется перпендикулярно плоскости расположения гибридных орбиталей. Эта р -АО участвует в образовании p-связи.

Для элементов 2-го периода процесс sp 2 -гибридизации происходит по схеме:
2s + 2p x + 2p y = 3 (2sp 2) 2p z -АО в гибридизации не участвует.

Для изображения пространственного строения атомов в sp 2 -состоянии используются те же приемы, что и в случае sp 3 -атомов:

Переход от орбитальной модели атома в sp 2 -гибридизированном состоянии (а) к пространственной формуле (б). Строение молекул с sp 2 -атомами отражают их модели:



Модели молекулы этилена
sp 2 -Гибридизованное состояние свойственно атому, если сумма числа связанных с ним атомов и числа его неподеленных электронных пар равна 3
Углерод в sp 2 -гибридном состоянии образует простое вещество графит. Это состояние характерно для атомов С, N, O и др. с двойной связью (sp 2 -атомы выделены красным цветом):
H 2 C =C H 2 , H 2 C =C HR, R 2 C =N R, R-N =N -R, R 2 C =O , R-N =O ,
а также для катионов типа
R 3 C + и свободных радикалов R 3 C · .




